Cardiomyopathie à caractère familial caractérisée par une infiltration adipeuse du myocarde et des fines plages de fibrose à la place des cellules myocardiques des couches épicardiques et médiomurales et qui atteint en priorité le ventricule droit. Mise en évidence par une équipe française en 1982 [1][1bis]. Sa prévalence est comprise entre 1/1000 et 1/5.000 atteignant de préférence les hommes jeunes [2][14]. Certaines causes sont clairement génétiques (ex. anomalie des desmosomes), en rapport avec une transmission autosomique dominante à pénétrance variable (parfois porteurs sains) avec rôle de facteurs environnementaux [3].
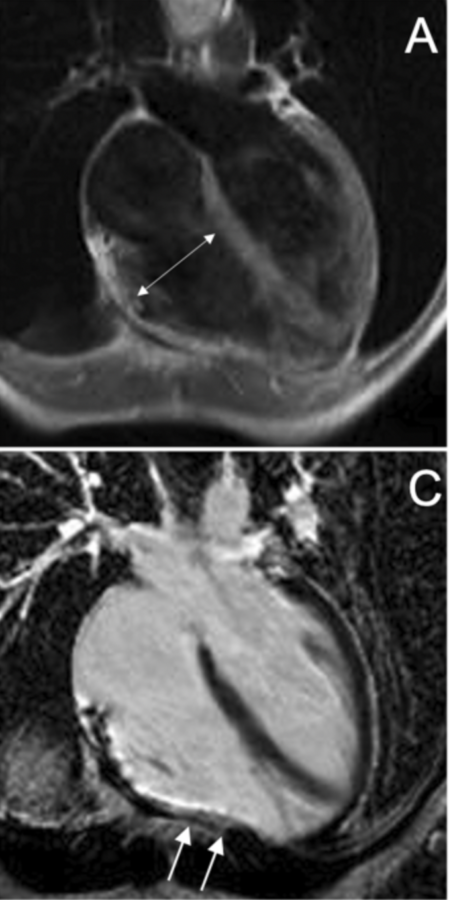
Elle entraîne une dilatation ventriculaire droite d’abord localisée, puis diffuse, qui évolue tardivement vers une insuffisance cardiaque et/ou une atteinte du ventricule gauche. Certaines atteintes sont limitées au ventricule gauche [3]. L’IRM est généralement l’imagerie de choix pour le diagnostic (cf. A. Cipriani, Eur Radiol 2023).
Les symptômes révélateurs (à partir de 25-30 ans) sont très variés, fatigue, palpitations, malaise/syncope ou défaillances cardiaques congestives, associées ou non à des anomalies du rythme. La survenue d’arythmies ventriculaires, parfois inaugurale, s’observe en particulier chez le sujet jeune avant 35 ans à la faveur d’un effort physique. Cette arythmie peut être la première manifestation de la maladie (cf. ECG du sportif). Elle peut parfois révéler une maladie familiale.
Synonyme. Cardiomyopathie ou dysplasie du ventriculaire droit arythmogène (CVDA ou DVDA) ou ” arrhythmogenic right ventricular cardiomyopathy “.
L’ECG est rarement pathognomonique
Il peut être normal au début (ou considéré à tort comme normal). Il peut parfois révéler la maladie en montrant certains signes qui prédominent en dérivations précordiales droites [4]. Ces signes dont la prévalence augmente avec le temps sont associés de façon variable [5] et leurs valeurs sémiologiques (critères mineurs ou majeurs) ont fait l’objet d’un consensus en 2010 (Marcus [5]), puis 2019 (Towbin [9]).
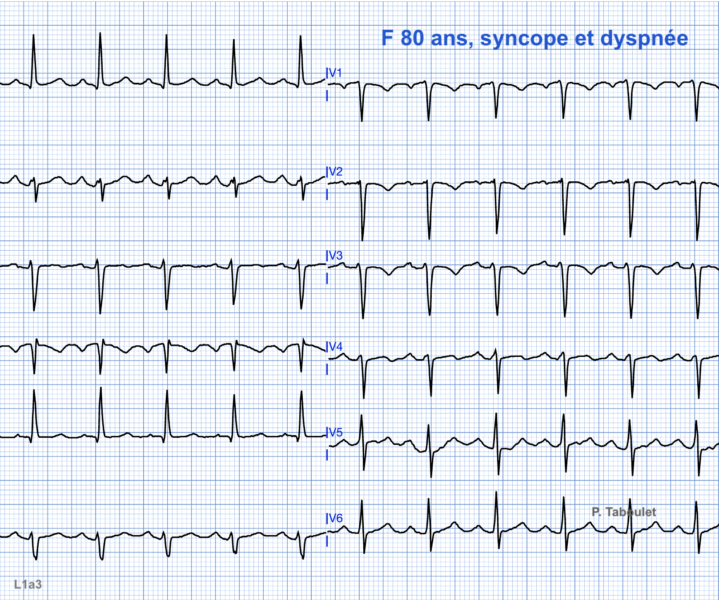
- Ondes T inversées
- de V1 à V3 ou au-delà, après 14 ans, en l’absence de BBD complet (critère majeur).
- ondes T inversées en V1-V2 ou bien en V4, V5 ou V6 en l’absence de BBD complet (critère mineur).
- ondes T inversées en V1-V4 , après 14 ans, en présence d’un BBD complet (critère mineur).
L’inversion des ondes T est quasi constante en fin d’évolution de V1 jusqu’en V5-V6, voire DIII-VF-DII. Les QRS qui précèdent sont rarement normaux (ondes R amples, QRS fragmentés ou RsR’, microvoltage, retard droit…) différents d’un bloc de branche droit [12]).

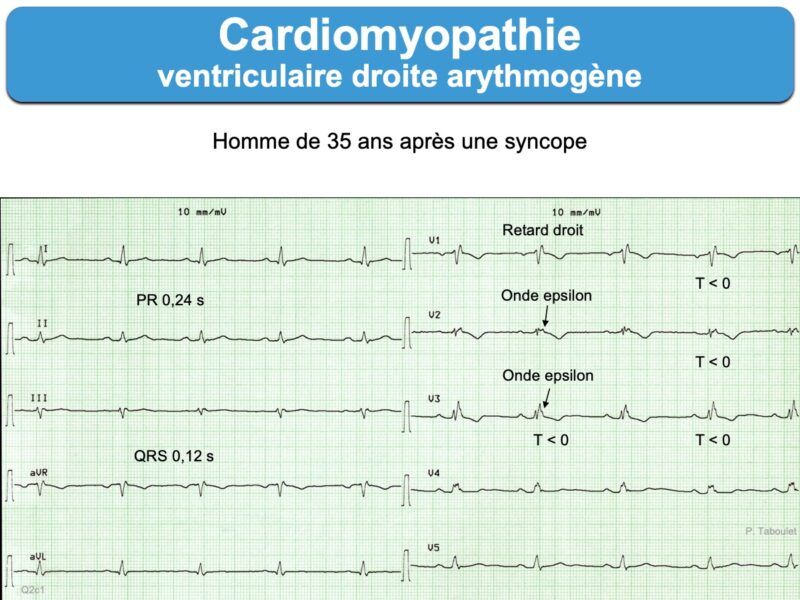
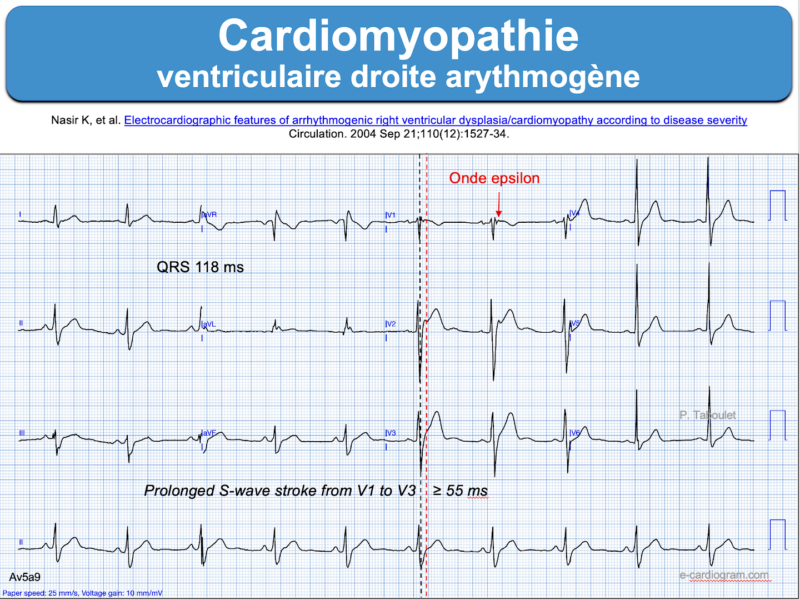
- onde epsilon dans une ou plusieurs dérivations précordiales droites (V1-V3). Sa présence (30% des cas) constitue un critère majeur de cardiomyopathie du VD. Son nom lui a été donné par un français, GH Fontaine en 1982, par opposition à l’onde delta qui précède le QRS [14]. C’est un signal de basse amplitude situé entre la fin du QRS et le début de l’onde T. C’est le seul signe pathognomonique, mais il est rarement visible au stade initial de la maladie et peut manquer au cours de l’évolution. Une loupe et de l’expérience sont souvent nécessaires pour la voir. Peu de cardiologues/urgentistes… savent reconnaitre une onde epsilon (sans formation spécifique, ils n’en feront probablement jamais le diagnostic ou passeront à côté s’il ne la recherche pas). L’onde epsilon peut s’observer uniquement en V1 ou dans d’autres dérivations (ex. V3R ou les dérivations inférieures) ou per tachycardie [15].
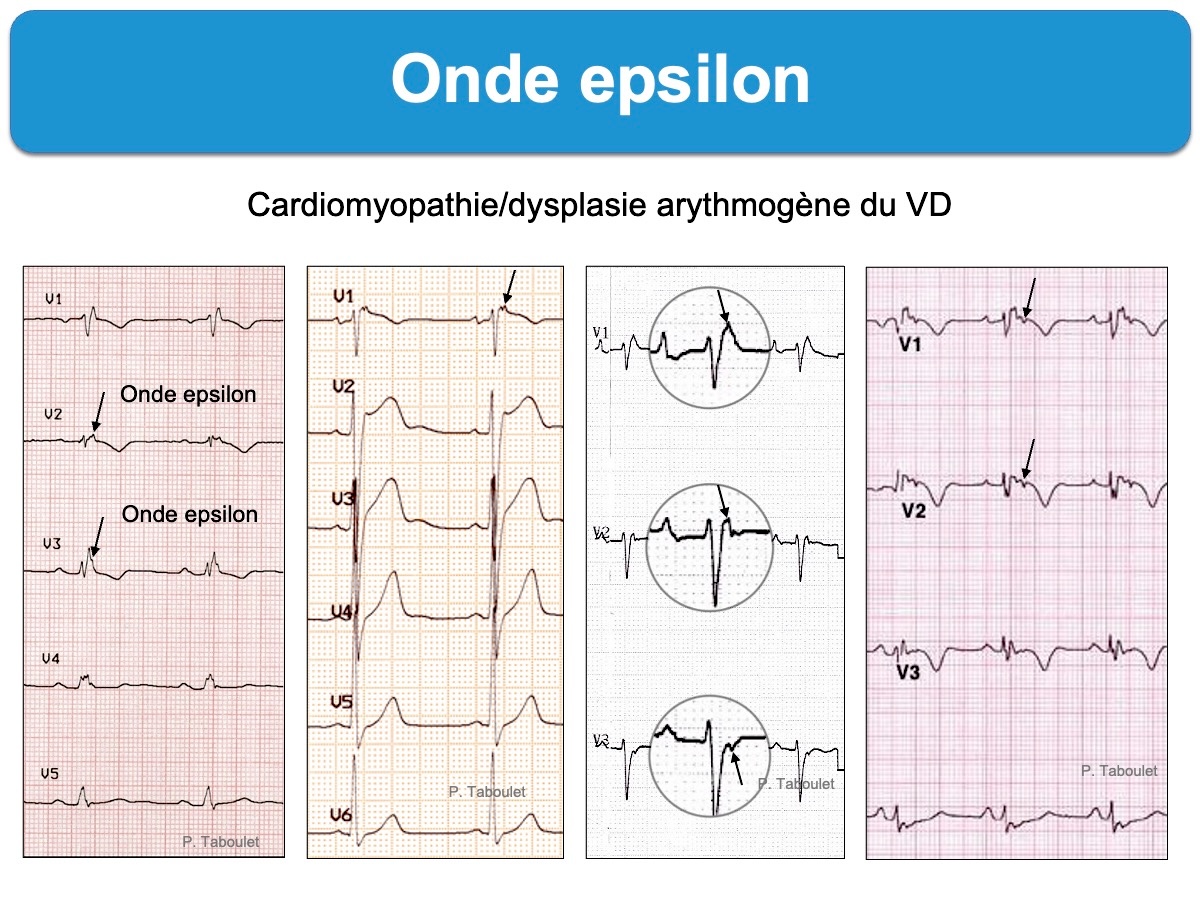
- bloc intraventriculaire focal (cf. QRS fragmentés) avec un allongement de la durée des QRS > 110 ms.
- Prolongation de l’activation terminale du QRS de V1 à V3 avec ascension prolongée de l’onde S ≥ 55 ms (prolonged S-wave upstroke) en l’absence de BBD. Cette durée se mesure à partir du nadir de l’onde S à la fin des déflexions du QRS, incluant une onde R’ ou une onde epsilon) [6]. Ce signe fréquent est un critère mineur qui témoigne de l’activation retardée du ventricule droit.
Signes associés
On observe fréquemment :
- un complexe QRS de durée plus longue en V1-V3 (ex. ≥ 25 ms) qu’en V5-V6 (« bloc plus que droit »).
- un bloc de branche droit complet dans les formes vues tardivement, souvent très atypique (QRS ≥ 120 ms mais microvolté avec une onde R’ plus large en V1 que l’onde S en V6 (mismatch) souvent déformé par une onde epsilon) [14],
- une déviation axiale droite. Une déviation axiale gauche est possible (liée à l’involution des vecteurs originaires du VD),

- une hypertrophie atriale droite est possible
- des QRS bas voltés ou microvoltés (< 0,5 mV) dans les dérivations frontales ou précordiales, de mauvais pronostic [13],

- des extrasystoles atriales ou une tachycardie/fibrillation atriale) [11],
- des extrasystoles ventriculaires à type de retard gauche (car issues du VD), fréquentes (> 500/24 h), souvent associées et parfois révélatrices (critère mineur)
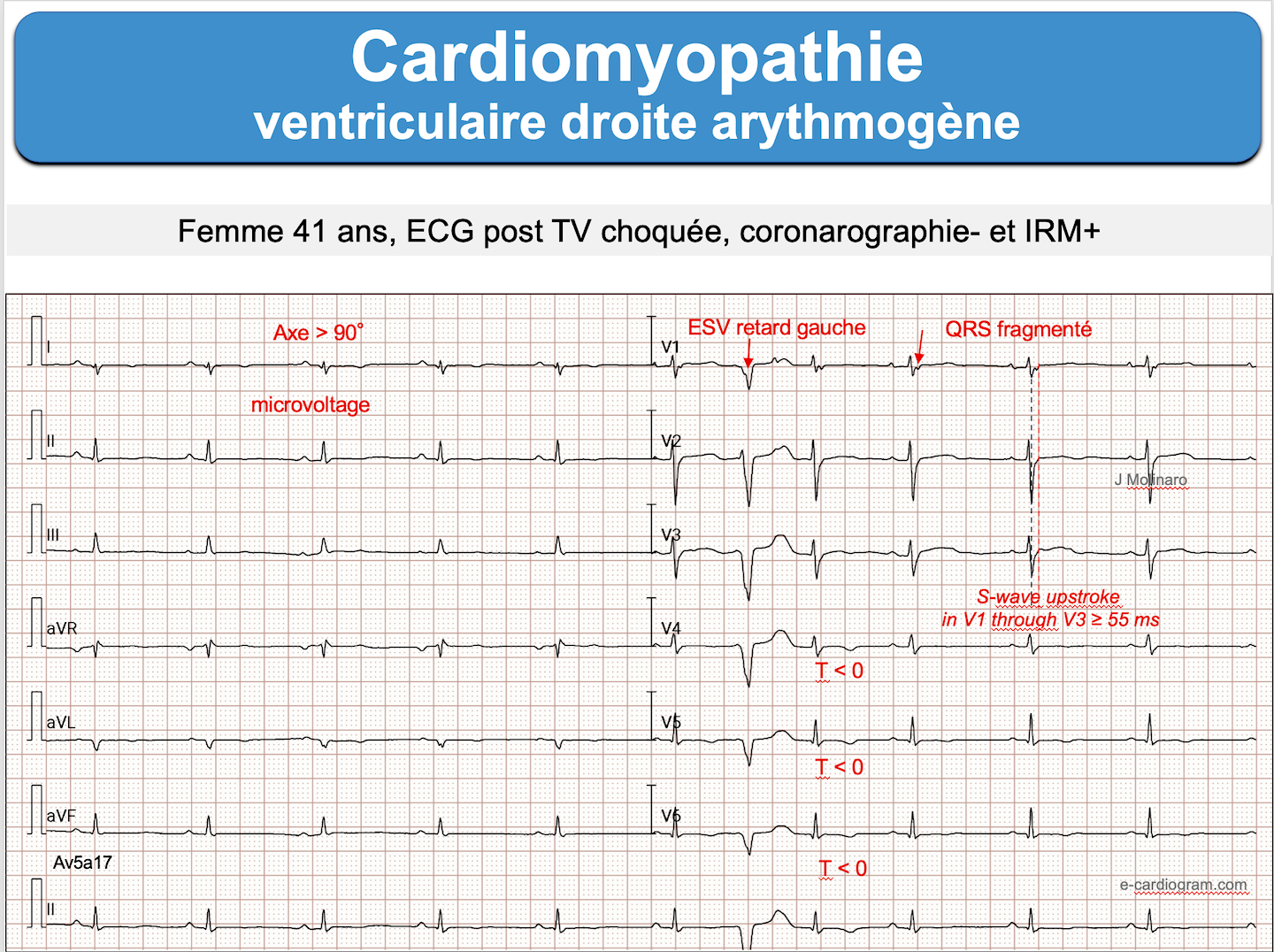
- des tachycardies ventriculaires, parfois révélatrices, de type retard gauche (car issue du ventricule droit) et axe supérieur (QRS positifs en dérivation VL), en contexte adrénergique lié au stress ou à l’effort (sport). –> Cardiomyopathie arythmogène : TV et aussi [10].

Les diagnostics différentiels
- Chez un sujet asymptomatique : la repolarisation juvénile et l’inversion bénigne de l’onde T
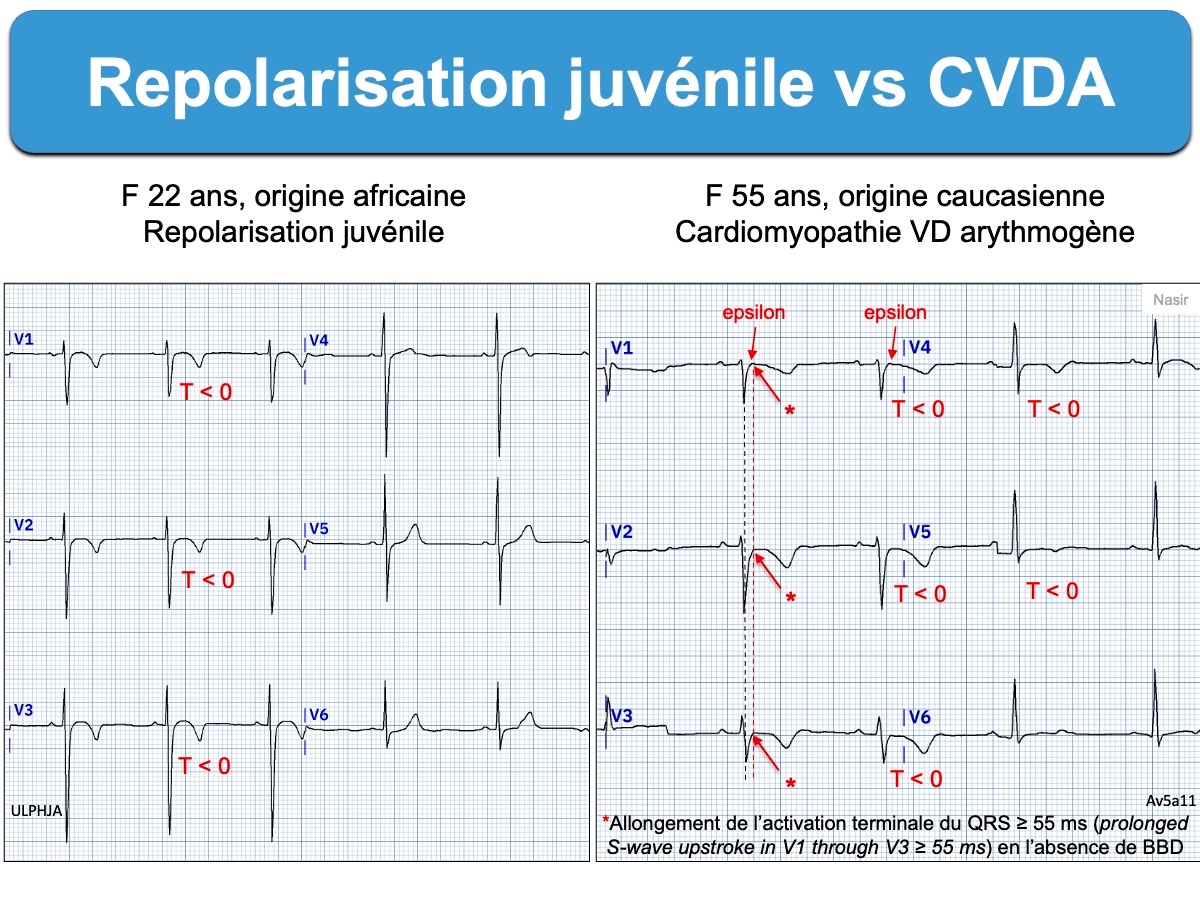
- En cas de dyspnée : une CIA, le cœur pulmonaire (ex. embolie pulmonaire) ou les cardiomyopathies dilatées
- Divers : certaines atteintes cardiaques dans le cadre de maladie neuromusculaire et la sarcoïdose cardiaque et plus rarement encore la maladie de Chagas, les myocardites.
Suspicion de CVDA ?
La prise en charge fait l’objet de consensus (2019) [9] et ESC 2022 [9bis]
L’évocation d’une CVDA doit conduire à :
- réaliser une imagerie (d’abord échocardiographie, puis surtout une IRM ou plus rarement une scintigraphie en contraste de phase),
- prise en charge en centre spécialisé pour les explorations complémentaires et le traitement préventif ou secondaire des arythmies ventriculaires ou de l’insuffisance cardiaque
- exploration fonctionnelle (ex. ECG à haute amplification pour la détection de potentiels tardifs ventriculaires,
- exploration électrophysiologique avec test isoprénaline, épreuve d’effort et/ou mapping électro-anatomique)
- voire exceptionnellement une biopsie endomyocardique
- interdire la pratique du sport intense et introduction de bêtabloquant
- dépistage génétique familial en centre spécialisé
En population pédiatrique [8] (2022, téléchargeable)
Vidéo Cardiogen – filière nationale de santé maladies cardiaques héréditaires ou rares Dysplasie Arythmogène du ventricule droit
Sites d’imagerie cardiaque des cardiopathies
Merci de me contacter si vous souhaitez améliorer ce contenu.
Références commentées réservées aux abonnés
La suite est réservée aux membres et stagiaires du site.
Se connecter | Devenir membre | Devenir stagiaire