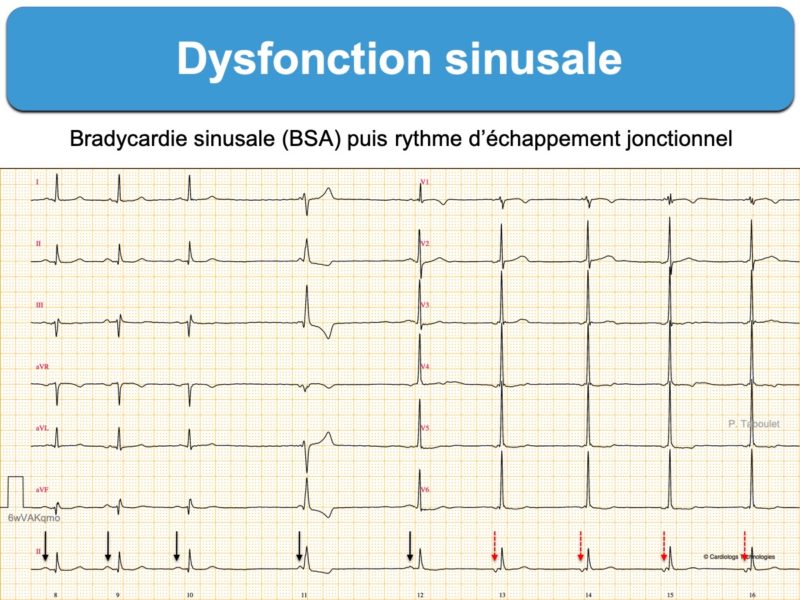
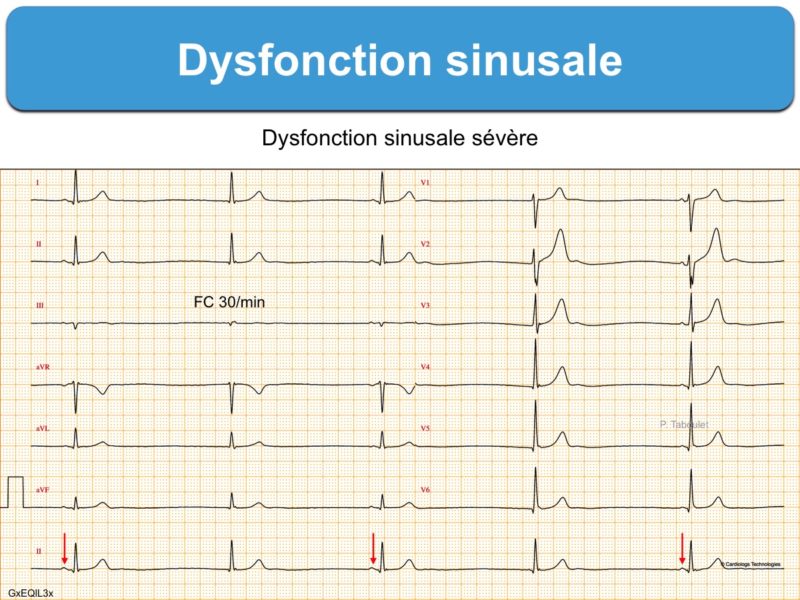
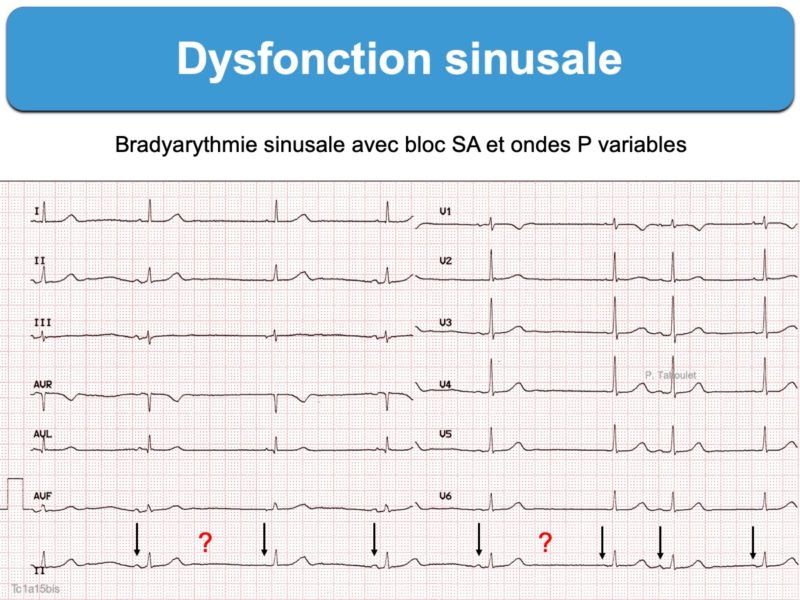
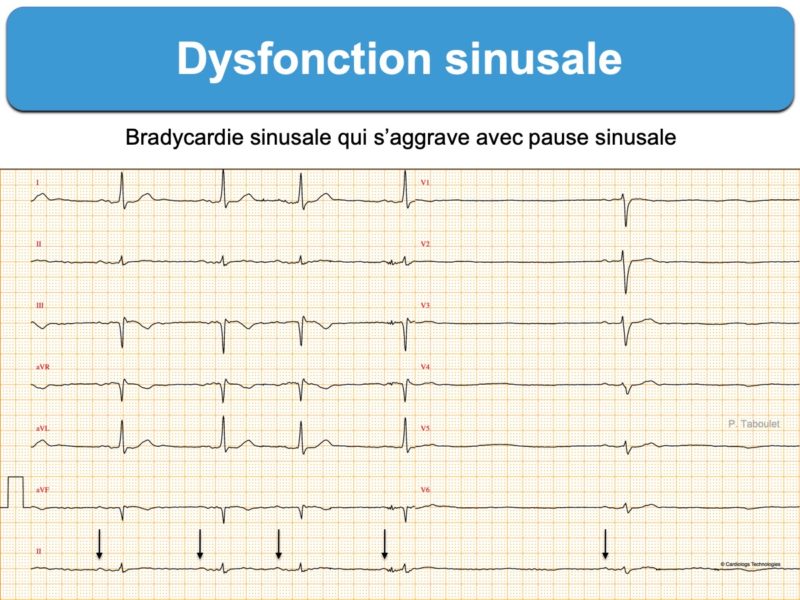
Anomalie de l’automatisme du nœud sinusal qui contrôle physiologiquement l’activation électrique du cœur.
Il s’agit en général d’une maladie des personnes âgées (sauf rares exceptions) en rapport avec la dégénérescence des fibres du nœud sinusal (sinus node dysfunction). Les patients présentent une fréquence cardiaque entre 50 et 40 bpm voire moins, ce qui s’accompagne de symptômes peu spécifiques comme une fatigue, une dyspnée d’effort, des étourdissements ou des palpitations. Un tableau d’insuffisance cardiaque congestive ou parfois une syncope peuvent révéler une dysfonction sinusale sévère.
L’ECG
La présentation ECG est très variée. Elle associe à des degrés divers [1]
- des anomalies de l’automatisme sinusal : bradycardie sinusale (< 50 bpm qui ne s’accélère pas à l’effort, Cf. bradycardie sinusale inappropriée), bradycardie atriale ectopique (ectopic atrial bradycardia), des épisodes de rythme d’échappement jonctionnel ou parfois un rythme d’échappement ventriculaire, des pauses ventriculaires > 3 secondes (absence d’onde P au hasard, sans relation avec le rythme sinusal), et au maximum une paralysie sinusale (sinus node arrest).
- des anomalies de la conduction intra-atriale : bloc sino-atrial (type bloc de sortie avec une pause ventriculaire égale exactement au double ou au triple de l’intervalle P-P en rythme sinusal), une réentrée intra-sinusale. Ces anomalies peuvent être à l’origine de tachycardie sinusale inappropriée ou de tachycardie supraventriculaire (typiquement une fibrillation atriale).
- une alternance de bradycardie sinusale sévère avec une tachycardie/fibrillation atriale appelée syndrome bradycardie-tachycardie (cf. Maladie rythmique de l’oreillette) ou syndrome du sinus malade (sick sinus syndrome).
Cause primitive par dégénérescence cellulaire
Les ondes P sont souvent lentes, peu voltées, allongées ou dysmorphiques, intermittentes parfois.
Des anomalies de l’automatisme des autres pacemakers et/ou de la conduction AV sont fréquemment associées (cf. Maladie rythmique de l’oreillette).
Le traitement des formes symptomatiques repose sur la stimulation ventriculaire par pacemaker.
Bien qu’un ECG à 12 dérivations soit généralement suffisant pour poser le diagnostic, un moniteur Holter de 24 heures ou un enregistreur d’événements de 30 jours peut être utile pour corréler le rythme lent avec les symptômes. Ces patients doivent être référés à un électrophysiologiste, car un stimulateur cardiaque est généralement nécessaire pour soulager les symptômes et prévenir la syncope. Aucun médicament ne peut aider à améliorer la fonction du nœud sinusal.
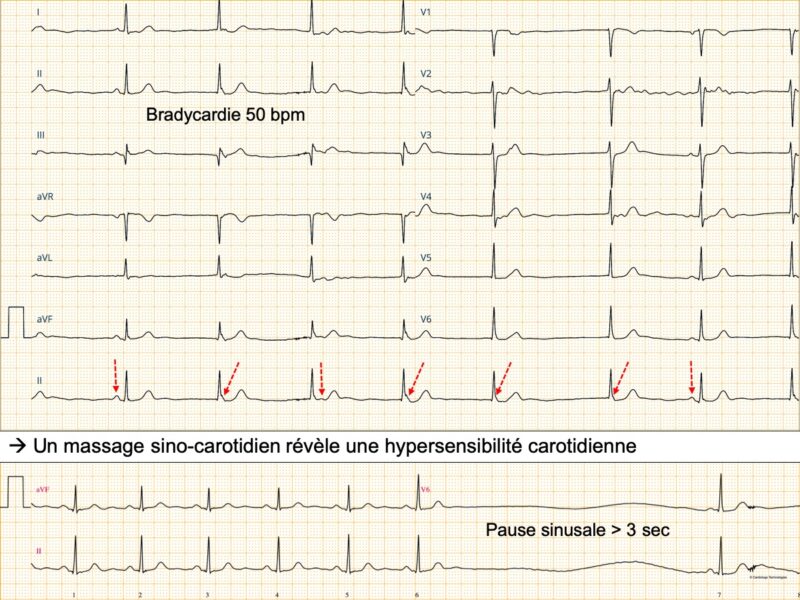
Un massage sino-carotidien peut révéler une hypersensibilité sino-carotidienne si survient une pause sinusale > 3 sec et en cas de symptômes associés, ce syndrome est une indication à la pose d’un stimulateur cardiaque, sans exploration complémentaire.
Causes secondaires réversibles
- médicaments. Ceux qui dépriment le nœud sinusal et en particulier l’amiodarone et la digoxine, mais aussi les bêtabloquants, certains antiarythmiques de classe I, les inhibiteurs calciques (vérapamil et diltiazem), la clonidine, la morphine, les dérivés opioïdes et certains psychotropes, certains anesthésiants sympatholytiques [4], le thalidomide…
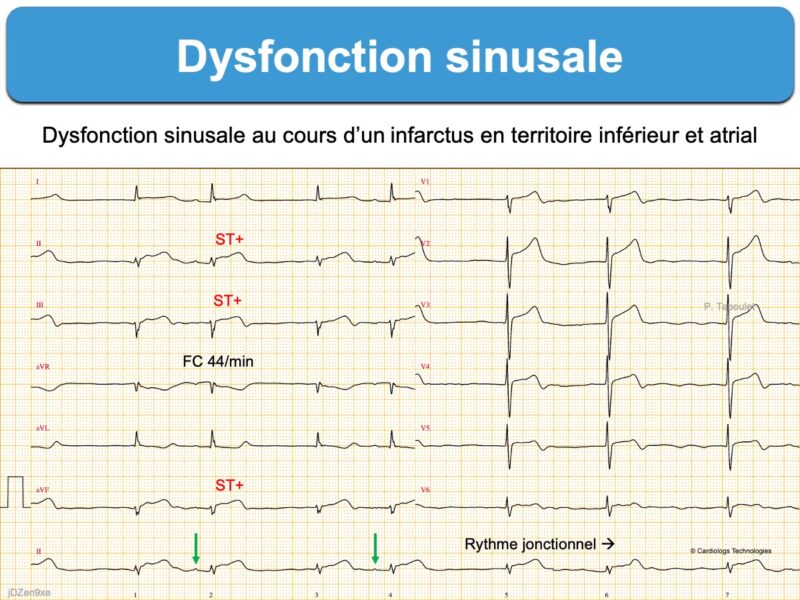
- infarctus. Territoire inférieur avec infarctus atrial droit
- hypertonie vagale.
- hyperkaliémie. Toujours y penser devant toute bradycardie ou tout trouble de conduction inexpliqué(e)
- hypothyroïdie.
Cause génétique ou congénitale (exceptionnelle)
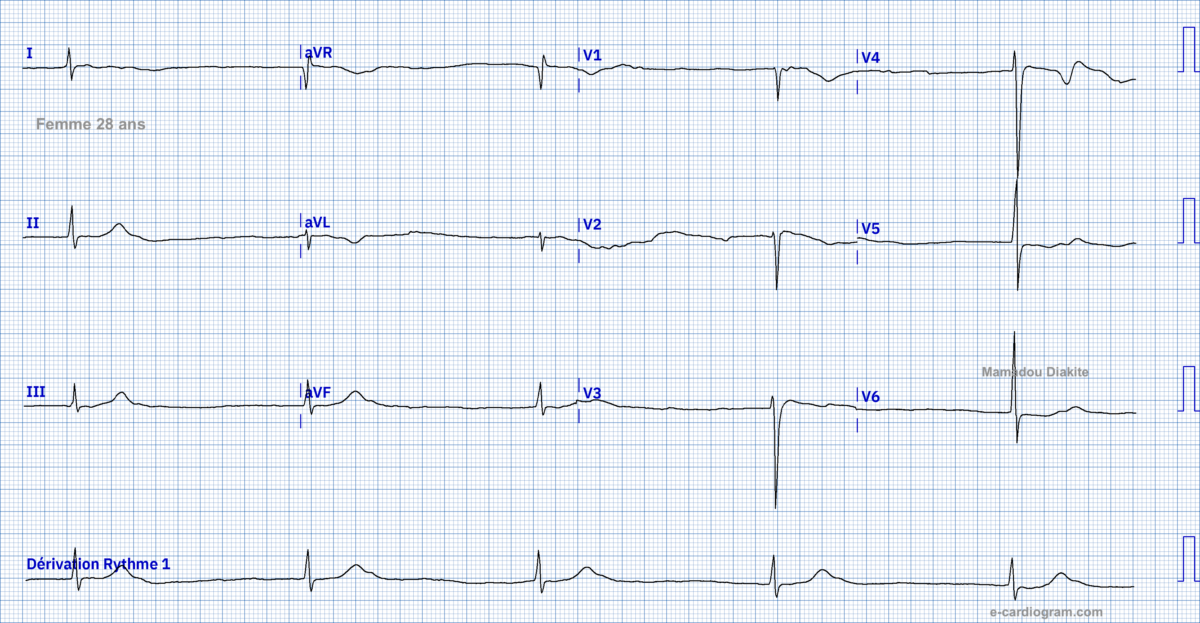
Ci-dessous le cas d’une femme de 28 ans dont l’oreillette est totalement inexcitable spontanément ou après stimulation atriale. Le rythme est jonctionnel lent (FC 28/min) très mal toléré, accéléré à 40/min après injection d’atropine.
[1] Kusumoto FM, Schoenfeld MH, Barrett C, et al.. 2018 ACC/AHA/HRS guideline on the evaluation and management of patients with bradycardia and cardiac conduction delay: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society. Circulation. 2019; 140:e382–e482. (téléchargeable)
[2] Taboulet P. La conduction intracardiaque. Partie 1. Physiopathologie et blocs de conduction supranodaux. AFMU 2014
[3] Byrnes TJ, Costantini O. Tachyarrhythmias and Bradyarrhythmias: Differential Diagnosis and Initial Management in the Primary Care Office. Med Clin North Am. 2017 May;101(3):495-506.
[4] Khanna S, Sreedharan R, Trombetta C, Ruetzler K. Sick Sinus Syndrome: Sinus Node Dysfunction in the Elderly. Anesthesiology. 2020 Feb;132(2):377-378. (téléchargeable) –> Autonomic imbalances from central neuraxial anesthesia–induced sympathectomy and use of sympatholytic drugs, such as propofol, remifentanil, dexmedetomidine, or vecuronium, during general anesthesia can unveil latent sinus node dysfunction and trigger life-threatening atropine-resistant bradyarrhythmias.