Les tachycardies atriales focales (TAF) sont un sous-ensemble de tachycardies atriales en rapport avec l’activation centrifuge de l’oreillette à partir d’une petite région atriale [1]. Elles peuvent survenir sur cœur sain, quel que soit l’âge, mais sont souvent associées à des anomalies structurelles. Elles représentent environ 5% des tachycardies supraventriculaires [2].
L’origine d’une TAF peut être n’importe où dans une oreillette, mais des sites particuliers de prédilection sont la crista terminalis, l’anneau valvulaire tricuspide et mitral, et dans les veines thoraciques rejoignant les oreillettes [1].
Les formes paroxystiques peu rapides sont fréquentes et souvent asymptomatiques, tandis que les accès soutenus rapides sont gênants et les formes chroniques peuvent avoir des conséquences hémodynamiques à court (lipothymie, palpitations, syncope ou malaise, embolie, insuffisance cardiaque) ou long terme (cf. Cardiomyopathie rythmique). Elles présentent des similitudes cliniques avec les tachycardies réciproques par réentrée (ex. Tachycardie de Bouveret et syndrome de WPW). Les accès peuvent être brefs, soutenus ou incessants avec des interruptions spontanées et des récurrences fréquentes [1].
La transformation de certaines TAF en fibrillation atriale ou en flutter atrial est possible et vice versa.
Triangle de Coumel
Le facteur gâchette (trigger) qui lance l’arythmie peut être une extrasystole, une accélération ou plus rarement un ralentissement de la fréquence des influx. D’autres triggers sont plus rares (la voix, la respiration, la toux) [11]. Le substrat arythmogène susceptible d’entretenir le trouble du rythme peut être une zone ischémique, de fibrose, ou de réentrée. Les modulateurs péjoratifs sont neuro-humoraux (en particulier une stimulation sympathique, ou une décharge de catécholamines), électrolytiques (hypokaliémie, hypomagnésémie), métaboliques (ischémie, acidose) ou médicamenteux (ex. digoxine, bêta-2…). Une perturbation de ces facteurs augmente la sensibilité du substrat et/ou facilite la conduction au sein du circuit (cf. Triangle de Coumel). Les mécanismes qui pérennisent les accès sont décrits plus bas.
Aspects ECG
Le diagnostic positif est souvent difficile sur un ECG 12 D de 10 secondes ou sur une salve de TA et encore plus difficile sur un ECG monopiste ou un Holter.
La tachycardie
- Elle est initiée habituellement par une extrasystole atriale dont la morphologie per tachycardie est similaire à celle constatée hors tachycardie [7].
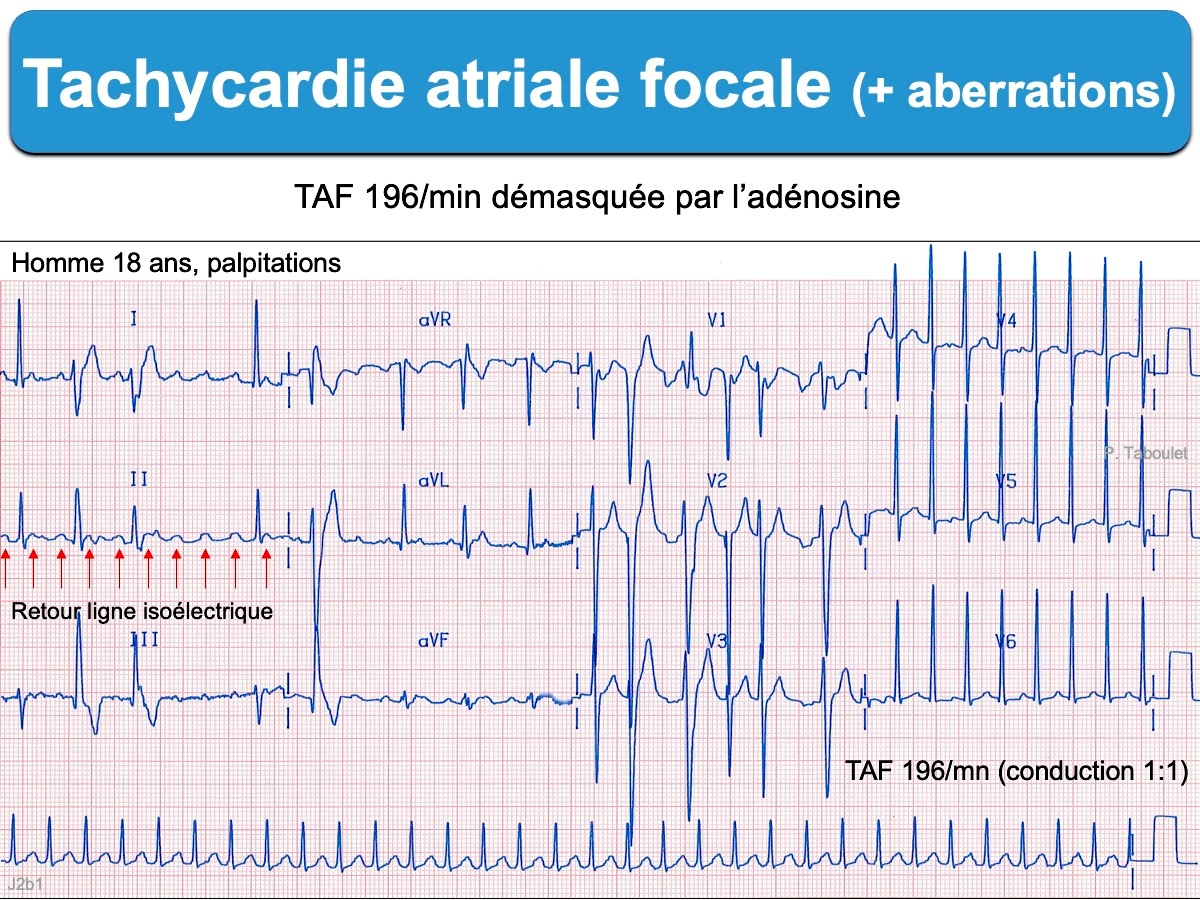
- L’activité atriale est monomorphe avec un retour à la ligne isoélectrique visible entre deux ondes P (critère majeur). Elle est généralement difficile à voir, car masquée dans les QRS et/ou dans les ondes T.
- L’activité atriale est régulière, mais le début et la fin de crise peuvent être progressifs (cf. Tachycardie atriale automatique)
- La fréquence atriale est comprise entre 130 et 250/min (mais certaines fréquences sont proches de 100/min; d’autres atteignent 300/min, en particulier chez l’enfant ou les sujets jeunes, non distinguables d’un flutter) [1][4].
NB. Une tachycardie régulière à QRS fins sans onde P visible est appelée tachycardie supraventriculaire
L’aspect des ondes P
L’aspect des ondes P (atriogramme), lorsqu’elles sont visibles, renseigne sur l’origine anatomique de l’influx ectopique [3][4][5].
- Les atriogrammes sont le plus souvent différents des ondes P sinusales (ex. « ondes P’ » amples et fines, petites et brèves ou négatives et profondes…).
- Les atriogrammes sont parfois similaires aux ondes P sinusales quand le foyer est proche du nœud sinusal (ex. crista terminalis ou veine pulmonaire supérieure droite) [2].
- Une onde P positive en DI et négative en V1 suggère une origine atriale droite [3].
- Une onde P négative en DI et aVL et positive en V1 suggère une origine atriale gauche [7].
- Les ondes P négatives dans les dérivations inférieures suggèrent une origine caudale,
- Les ondes P positives dans les dérivations inférieures suggèrent un emplacement supérieur [2][3][4].
L’aspect de l’onde P qui initie ou termine la tachycardie (cf. TAF par réentrée), l’évolution (avec warm up et cool down de la TAF automatique) et le mode de terminaison, spontané ou sous l’action de l’adénosine ou de manœuvres vagales apportent des renseignements sur le mécanisme électrophysiologique [1][5].
Un mapping peut être utilisé pour aider à localiser le site à l’origine de la tachycardie avant l’ablation.
L’intervalle PR et le ratio P/QRS
L’intervalle R-P est typiquement long (intervalle R-P = intervalle P-R) et variable selon la fréquence atriale, mais il peut être normal et constant, voir court lorsque l’onde P commande le QRS +2.
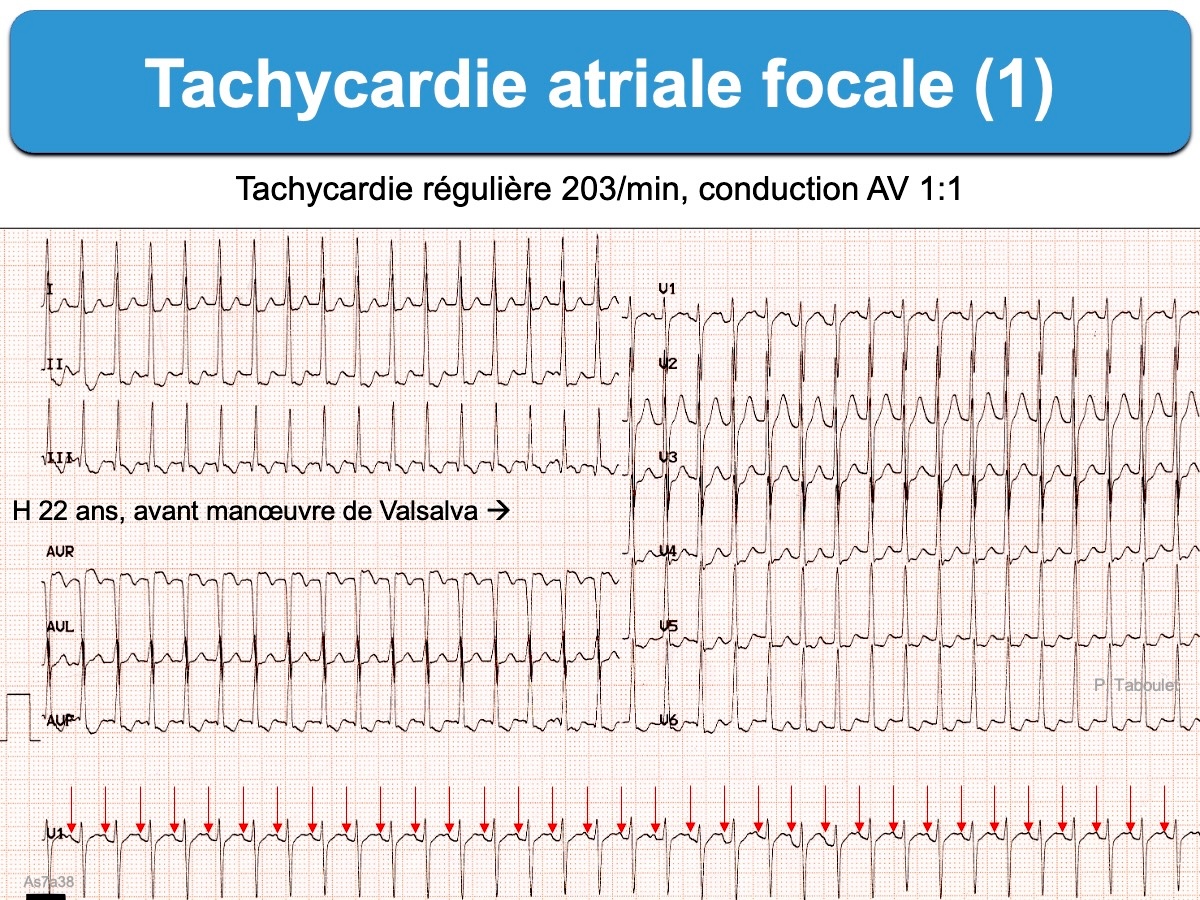
- Le ratio P/QRS est généralement = 1, mais il varie selon la fréquence atriale et les propriétés du nœud AV.
- Un ratio P/QRS > 1 est utile pour écarter le diagnostic différentiel fréquent de tachycardie jonctionnelle.
- Quand le ratio P/QRS = 2, le diagnostic différentiel avec un flutter atrial est quasi impossible sur l’ECG sans recourir aux données de l’électrophysiologie intracavitaire [4].
- Le ratio P/QRS est parfois variable (ex. 3:2 ou 4:1) en cas de bloc AV nodal associé (ex. bêtabloquant, digitalique, amiodarone…)

- Le ratio P/QRS peut être encore plus variable, en cas de freinage de conduction à plusieurs niveaux (multilevel block).

L’axe et la morphologie des QRS
- Les QRS sont généralement identiques à ceux qui entraînent l’activité sinusale physiologique.
- Néanmoins, un élargissement des complexes QRS est possible, en particulier au cours des fréquences atriales rapides ou/et variables, lorsqu’une des branches de conduction est en période réfractaire (cf. Bloc de branche fonctionnel ou aberration).
- Des anomalies secondaires de la repolarisation (liées à la cadence ventriculaire rapide) sont habituelles et peuvent persister quelques minutes-heures, après retour en rythme sinusal.
Les mécanismes responsables [1][5]
- A. une activité autodéclenchée (cf. post-dépolarisation) : mécanisme le plus fréquent
- B. une microréentrée (microzone de conduction anormale ou anisotropie)
- C. un automatisme anormal (cf. TAF automatique) : plus rare
Les mécanismes liés à une réentrée peuvent être sensibles aux manœuvres vagales. Voir ci-dessous.
‘ECG et parfois même l’exploration endocavitaire ont des limites pour expliquer avec certitude le mécanisme précis [5].
En faveur d’une micro-réentrée
Le cœur est généralement sain, mais des anomalies structurelles peuvent servir de substrat arythmogène (micro zones de conduction lente et anisotropie) ce qui explique que l’âge moyen soit plus élevé que pour les TAF automatiques et la prévalence des maladies pulmonaires. Les TAF peuvent aussi s’intégrer dans le cadre d’une dysfonction sinusale.
Sur l’ECG, une TAF par microréentrée est suspectée devant [3][4]:
- Une fréquence atriale entre 120 et 200/min, avec un début et une fin brusques, ce qui la distingue d’une tachycardie sinusale inappropriée. La fréquence atriale varie peu contrairement aux TAF automatiques [6].
- Un allongement de l’intervalle P-R lors du début de l’accès (cf. Conduction décrémentielle du nœud AV)
- Un atriogramme différent de l’onde P sinusale, sauf si la réentrée est limitée à la région intra ou parasinusale (« tachycardie sinoatriale » ou « réentrée intrasinusale »). Le premier atriogramme peut changer légèrement d’aspect au début de l’accès en raison des modifications induites par la réentrée.
- Une conduction AV généralement bonne (1:1), mais qui peut être dégradée spontanément (bloc AV fonctionnel) ou sous l’action de médicament ralentisseur (ex. conduction 2:1 ou 3:2).
- Des QRS fins, sauf en cas d’aberration ventriculaire fréquence-dépendant ou de bloc de branche préexistant [10].
La distinction entre microréentrée et activité déclenchée comme mécanisme de TAF est quasi impossible en clinique, d’autant que l’adénosine souvent inefficace sur la microréentrée [7] peut parfois stopper les deux types et la stimulation électrique programmée les déclencher toutes deux.
Le rôle déclenchant d’un surdosage en digitalique doit être connu.
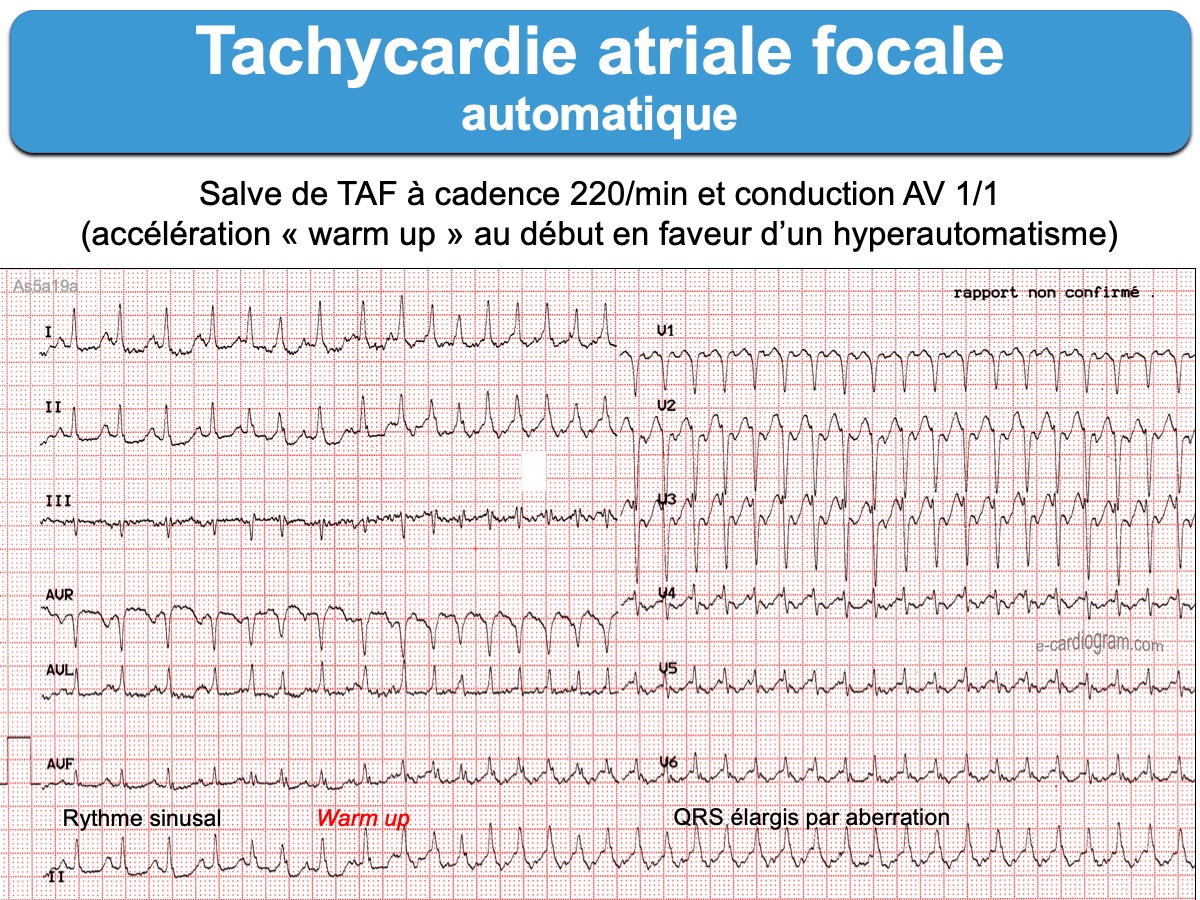
En faveur d’un automatisme –> TAF automatique
Diagnostics différentiels
Il est généralement très difficile sur un seul tracé d’affirmer qu’il s’agit d’une TAF.
- Une TAF peu rapide peut être prise pour une tachycardie sinusale. Une TAF a un début et une fin brusques, des ondes P souvent légèrement différentes du rythme sinusal et parfois une dissociation entre les 2 activités [1].
- Il faut évoquer un flutter atrial quand la fréquence atriale (ou ventriculaire) est ≥ 240/min, une fibrillation atriale quand les ondes P sont peu voltées et la conduction AV anarchique ou irrégulière, une tachycardie AV par réentrée intranodale quand les ondes P ne sont pas visibles ou que l’intervalle R-P est ≤ 90 ms ou une autre tachycardie atrioventriculaire par réentrée si l’intervalle R-P est long (> 90 ms voire R-P > P-R). Le diagnostic différentiel avec une tachycardie jonctionnelle n’est souvent possible qu’au cours d’une exploration électrophysiologique.
- Quand le diagnostic est incertain, il faut parler de « tachycardie supraventriculaire » ou de « tachycardie atriale ». Les renseignements fournis par les modes d’initiation et de terminaison de la tachycardie, les manœuvres vagales, un médicament déprimant la conduction AV (cf. Adénosine) et/ou l’enregistrement atrial par dérivation œsophagienne permettent généralement le diagnostic. On peut exclure une TAF si on montre que l’oreillette n’est pas obligatoire pour initier et perpétuer la tachycardie (ex. Capture sinusale) [5].
- Quand les QRS sont larges, le diagnostic est encore plus difficile et il faut évoquer une tachycardie ventriculaire, une imprégnation en flécaïnide [10], un effet stabilisant de membrane, une réentrée sur pacemaker… (cf. Tachycardie à QRS larges).
Les formes frontières
- les tachycardies sinusales inappropriées
- le rythme atrial accéléré
- une tachycardie par réentrée sino-atriale (fréquence habituelle 120/min, mais parfois lente ou plus rapide, onde P’ similaire à l’onde P sinusale, ratio RP’/P’R ≥ 1, début et fin brusques, arrêt par manœuvres vagales, sensibles aux antiarythmiques classe I) [8]
- la tachycardie atriale multifocale
Faites des quiz sur le site web (plusieurs niveaux de connaissance 1 à 3).
Femme jeune. Accès de palpitations bien tolérées. Pas de cardiopathie. Tachycardie sinusale ?

Réponse au quiz. Ci-dessous
Si vous souhaitez améliorer cette page, contactez-moi, merci
Traitement (ESC 2019) [2]
Le traitement des accès paroxystiques repose sur l’algorithme de cardioversion d’une tachycardie régulière [2]
Les manœuvres vagales, l’adénosine, les inhibiteurs calciques (et la cardioversion électrique) sont efficaces en cas de réentrée ou activité déclenchée, les bêtabloquants (IV ou PO) en cas d’activité autodéclenchée (hémodynamique stable et en l’absence d’insuffisance cardiaque), les antiarythmiques de classe Ic ou III en cas d’automatisme anormal (Classe IIa niveau C) (sauf CI). Le maintien en rythme sinusal à l’aide des bêtabloquants ou des inhibiteurs calciques (Classe I niveau C) ou autre traitement (ibutilide, propafénone ou flécaïnide) est souvent difficile.
Les formes récurrentes ou incessantes font appel aux méthodes ablatives (Classe I niveau B).
La place des anticoagulants est mal définie.

ECG de A Z (P. Taboulet 2ed 2025) : https://www.livres-medicaux.com/auteur/11567-taboulet
YouTube : ma playlist
Références et réponse au quiz
La suite est réservée aux membres et stagiaires du site.
Se connecter | Devenir membre | Devenir stagiaire
La suite est réservée aux membres et stagiaires du site.
Se connecter | Devenir membre | Devenir stagiaire